خلاصه
استفاده از گاز هیدروژن به عنوان وسیله ای برای جدا کردن عرضه از تقاضا برای انتقال به منابع انرژی بدون کربن و چشم انداز انرژی سبزتر و توزیع شده بسیار مهم است. این کار نشان میدهد که چگونه میتوان از پوششهای نیترید تیتانیوم در دسترس تجاری برای افزایش طول عمر الکترودهای فولاد ضد زنگ درجه ۳۱۶ برای استفاده به عنوان کاتد در سلولهای الکترولیز قلیایی استفاده کرد. این ماده با هدف ویژه ارزیابی مناسب بودن پوشش برای استفاده با منابع انرژی تجدیدپذیر متناوب، در معرض پیری سریع قرار گرفت. بیش از 2000 سیکل به مدت 5.5 روز، یک سلول الکترولیتی دارای پوشش 250 میلی ولت از سلول کنترل بهتر عمل کرد و کاهش بیش از حد پتانسیل در کاتد 400 میلی ولت مشاهده شد. این کار همچنین تأیید می کند که پوشش صرفاً برای استفاده کاتدی مناسب است و تجزیه و تحلیلی از تغییرات سطحی را ارائه می دهد که در صورت استفاده آندی از آن رخ می دهد.
کلید واژه ها:
نیترید تیتانیوم ؛ فولاد ضد زنگ ؛ الکترولیز قلیایی ؛ ذخیره انرژی
1. معرفی
با توسعه پوششهای الکترود با کارایی بالا برای تقسیم آب در دمای اتاق، شرایط قلیایی به عنوان وسیلهای برای ذخیره انرژی تجدیدپذیر اضافی به عنوان گاز هیدروژن از اهمیت بالایی برخوردار است [ 1 ، 2 ]. استفاده از گاز هیدروژن برای جدا کردن عرضه از تقاضا برای انتقال به منابع متناوب انرژی تجدیدپذیر و چشم انداز انرژی سبزتر بسیار مهم است [ 3 ، 4 ]. الکترولیز قلیایی جایگزینی برای الکترولیز غشای تبادل پروتون (PEM) بدون هزینههای بالا، در حالی که کارایی بالا را حفظ میکند، فراهم میکند [ 5 ، 6 ]. ذخیره انرژی ارزان و کارآمد از طریق تبدیل به هیدروژن باعث ایجاد یک چشم انداز انرژی پایدار می شود که به موجب آن چندین ورودی انرژی توزیع شده در مقیاس کوچک به سیستم وارد می شود، در مقایسه با سیستم «یک به چند» که اکنون منسوخ شده است. نیروگاه واحد به بسیاری از خانه ها و مشاغل تغذیه می کند. با توجه به ماهیت متناوب ورودیهای انرژی سبز، رویکرد «خیلی به چند» بسیار انعطافپذیرتر و پایدارتر است.
این مقاله به بررسی پایداری الکترود و پتانسیل طول عمر برای فولاد ضد زنگ و تنظیم الکترود نیترید تیتانیوم با پوشش تجاری میپردازد. ترکیب فولادهای ضد زنگ با استانداردهای بین المللی کنترل می شود و به طور گسترده ای در دسترس هستند، و آنها را به منبع مقرون به صرفه ای از یک ماده زیرلایه قابل اعتماد تبدیل می کند. مطمئناً آنها نسبت به زیرلایه نیکل خالص در دسترس و مقرون به صرفه تر هستند. رایج ترین گریدهای مورد بررسی برای الکترولیز 304 (304SS) و 316 (316SS) [ 7 ، 8 ، 9 ] هستند که هر دو عمدتاً از آهن، نیکل و کروم تشکیل شده اند، اما علاوه بر این، 316SS دارای درصد بیشتری از Ni است. تا حدود 2.5 درصد وزنی مو. این 316SS مقاومت بیشتری در برابر خوردگی ایجاد میکند، و آن را به اولین انتخاب برای کاربردهای دریایی و پزشکی تبدیل میکند، اما همچنین گرانتر و به طور بالقوه به دست آوردن چسبندگی پوشش را دشوارتر میکند. از نتایج گزارش شده توسط Carta و همکاران. یک مازاد پتانسیل برای یک کاتد 316SS 0.34- ولت در 10 میلی آمپر سانتیمتر مربع مشاهده شد [ 8 ]، اما برای نویسندگان در استفاده طولانیمدت مشخص شده است که حتی 316SS نیز خوردگی کاتدی قابلتوجهی را تجربه خواهد کرد (شکل 7 را ببینید).
نیترید تیتانیوم به دلیل رسانایی حرارتی و الکتریکی بالا، علاوه بر سختی مکانیکی آن [ 10 ]، و برای افزایش طول عمر الکترود برای واکنشهای کاهش اکسیژن و هیدروژن در یک سلول سوختی غشای تبادل پروتون شناخته شده است [ 11 ]. با این حال، بر اساس دانش ما برای استفاده با الکترولیز قلیایی متناوب بررسی نشده است، بنابراین این کار اولین مطالعه در نوع خود است. علاوه بر این، به طور گسترده ای به عنوان یک سرویس پوشش سفارشی برای افزایش طول عمر ماشین ابزار، در کنار پوشش های جایگزین مانند CrN، TiAlN و WS 2 در دسترس است [ 12 ]. در این زمینه، پوششها به دلیل سختی شدید و توانایی مقاومت در برابر اکسیداسیون در دماهای بالای تولید شده در حین ماشینکاری (که میتواند بیش از 800 درجه سانتیگراد باشد) انتخاب میشوند. این ویژگیها برای الکترولیز قلیایی در دمای اتاق نگرانی ثانویه دارند، اما در دسترس بودن و دسترسی گسترده به پوششها باعث میشود که به طور بالقوه مقرون به صرفه باشند. با این حال، باید دید که کدام (در صورت وجود) از این پوشش ها، مبادله بهینه بین عملکرد و هزینه را تشکیل می دهد. این مطالعه بر روی نیترید تیتانیوم تمرکز خواهد کرد.
پیری تسریع شده
طول عمر الکترود اغلب در متون علمی با استفاده از جریانهای ثابت مورد مطالعه و گزارش قرار میگیرد، که مسلماً کاربرد محدودی در زمینه جذب متناوب انرژی تجدیدپذیر دارند. استفاده متناوب به رسمیت شناخته شده است که نقش مهمی در تجزیه الکتروکاتالیست ها، به ویژه آنهایی که شامل نیکل هستند، ایفا می کند [ 13 ]. بنابراین، برای دستیابی به پیری سریع، نه تنها لازم بود که الکترودها را در مجموع مقادیر زیادی جریان قرار دهیم، بلکه در معرض چرخههای مخرب روشن و خاموش ناشی از طبیعت متناوب انرژی تجدیدپذیر نیز قرار گرفت. رژیمی ابداع شد که شامل 2 دقیقه روشن و به دنبال آن 2 دقیقه در شرایط مدار باز بود که به الکترودها زمان کافی برای شارژ و تخلیه کامل در هر چرخه، اعمال تنش خورنده در هر تغییر فاز، اجازه میداد. الکترولیز در دمای اتاق به این دلیل انتخاب می شود که بیشتر برای کاربردهای انرژی تجدیدپذیر کاربرد دارد، جایی که تقاضای متناوب به این معنی است که گرمایش دائمی الکترولیت ناپایدار است.
2. مواد و روشها
2.1. الکترودها
الکترودهای مورد استفاده همه فولاد ضد زنگ درجه 316 با ضخامت 0.9 میلیمتر برش خورده به اندازه و شکل، یا به صورت عرضه شده یا پوشش داده شده در TiN با استفاده از یک آمادهسازی تجاری استاندارد که پوشش TiN با ضخامت 1 تا 4 میکرومتر را ارائه میدهد. پوششهای تجاری نیترید تیتانیوم توسط Wallwork Cambridge Ltd., UK اعمال شد و مشخصات داخلی آنها برای پوشش “TIN COAT SPEC 300 1-4 MICRONS” بود. به منظور احترام به مالکیت معنوی شرکت، هیچ تلاشی برای مهندسی معکوس پوششها صورت نگرفته است، بنابراین نمیتوان در این تحقیق گزارش داد که چگونه ضخامت پوشش ممکن است بر عملکرد تأثیر بگذارد. انتظار نمی رود که تفاوت در ضخامت پوشش بالاتر از 1 میکرومتر باعث تغییرات قابل توجهی شود. این به این دلیل است که ماده رسانای الکتریکی است و از آنجا که چنین ضخامتی هزاران اتم را تشکیل می دهد، بعید است که بر شیمی سطح تأثیر بگذارد.
2.2. سالخورده
تمام آزمایشهای پیری با استفاده از منبع تغذیه جریان ثابت، متصل به یک سلول الکترولیتی لایهبندی شده دو الکترود، که عمدتاً از پلاستیک اکریلیک برش لیزری تشکیل شده بود، انجام شد ( شکل 1 را ببینید ) [ 14 ]. یک غشای Zirfon™ برای جدا نگه داشتن گازهای تکامل یافته استفاده شد و فاصله بین الکترودها تقریباً 30 میلی متر بود [ 5 ]. دو پروتکل مختلف پیری، همانطور که در جدول 1 شرح داده شده است، دنبال شد . مشاهده شد که در چگالی جریان بالاتر، یک الکترولیت قویتر برای حفظ افت ولتاژ کل در سراسر سلول الکترولیتی، و همراه با آن گرمایش اهمی مرتبط، در محدودههای معقول مورد نیاز است. انتخاب استفاده از NaOH به جای KOH معمول تر به این دلیل انجام شد که ارزان تر است و بنابراین برای کاربردهای تجاری کاربردی تر است. همچنین، با وجود اینکه برگه اطلاعات ایمنی بیان می کند که هرگز نباید آن را در زهکشی انداخت، اما به طور گسترده ای به عنوان پاک کننده فاضلاب شناخته شده و مورد استفاده قرار می گیرد و بنابراین نشت یا نشت تصادفی به فاضلاب یک خطر زیست محیطی قابل کنترل است.
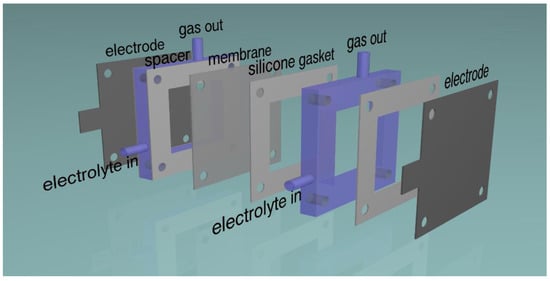
شکل 1. طراحی معمولی سلول الکترولیتی تجربی، بر اساس اجزای برش لیزری.
جدول 1. پروتکل های مختلف پیری تسریع شده به کار گرفته شده است.
هر آزمایش بین 5.5 تا 7 روز به طول انجامید. از چرخه های 4 دقیقه ای تشکیل شده است. در برخی آزمایشها، الکترولیت از طریق یک محفظه خارجی با استفاده از یک پمپ کوچک بدون جاروبک به گردش در میآمد.
2.3. سه آزمایش الکترود
همه آزمایشهای سه الکترودی بر روی یک پتانسیواستات n-Stat Ivium (آیندهوون، هلند)، متصل به طرح مشابهی از سلول الکترولیتی انجام شد. سطح الکترود کار (WE) با چسباندن یا پیچ کردن الکترود به ورق برش لیزری از اکریلیک شفاف 3 میلی متری حاوی یک پنجره 3 × 3 سانتی متر به 9 سانتی متر مربع کاهش یافت. الکترود شمارنده یک صفحه فولادی ضد زنگ 316 بود (که 6 × 6 سانتی متر آن در معرض دید قرار گرفت)، و الکترود مرجع (RE) یک طرح تجاری بود که شامل یک سیم Ag/AgCl معلق در KCl 3 M بود. فاصله بین الکترودهای کار و شمارنده تقریباً 15 میلی متر بود. الکترولیت 0.5 مولار NaOH (درجه معرف استاندارد) بود و آب دیونیزه شده در سراسر آن استفاده شد. قبل از هر آزمایش RE در برابر یک الکترود کالامل استاندارد (SCE) بررسی شد و الکترولیت به مدت 10 دقیقه با نیتروژن حباب شد تا اکسیژن محلول کاهش یابد. تمام آزمایشها در دمای محیط آزمایشگاه که 1 ± 20 درجه سانتیگراد بود انجام شد.
2.4. شیب تافل
روشی که توسط استیونز و همکاران بیان شده است. برای به دست آوردن اندازه گیری های شیب تافل دنبال شد [ 15 ]. این شامل مراحل کرونوپتانسیومتری در چگالی و مدت زمان متغیر است که در جدول 2 مشخص شده است .
جدول 2. چگالی جریان و مدت زمان برای تجزیه و تحلیل تافل.

هر اجرای آزمایشی شامل هر دو شیب تافل صعودی و نزولی بود که کل روند دو بار تکرار شد. نتایج منتشر شده از شیب نزولی اجرای دوم گرفته شده است.
2.5. تصحیح iR
به منظور تصحیح تلفات ولتاژ در الکترولیت بین الکترودهای مرجع و کار، طیفسنجی الکترو امپدانس (EIS) بین 100 هرتز و 1 مگاهرتز انجام شد. سپس مقاومت سری الکترولیت بهعنوان بزرگی نقطه نزدیکترین نقطه به مبدأ نمودار نایکیست به دست آمده تعریف شد. سپس افت ولتاژ در الکترولیت را می توان به سادگی با ضرب این مقاومت در جریان کل سلول خنثی کرد.
2.6. میکروسکوپ الکترونی
تصویربرداری میکروسکوپ الکترونی روبشی (SEM) و طیفسنجی پراکنده انرژی (EDX) بر روی یک طیفسنج AZtecOne Oxford Instruments (آکسفورد، انگلستان) متصل به میکروسکوپ رومیزی TM3030 هیتاچی (توکیو، ژاپن) انجام شد.
3. نتایج و بحث
آزمایشهای ولتامتری چرخهای نشان داد که پوشش TiN نمیتواند بهعنوان آند، حتی برای دورههای کوتاه، مورد استفاده قرار گیرد، که با یافتههای قبلی مطابقت دارد [ 16 ، 17 ]. پتانسیل الکتریکی مثبت باعث شد که پوشش به سرعت از رنگ طلایی اولیه به قهوه ای نارنجی تنها در چند ده ثانیه تغییر کند که با از دست دادن اکثریت رسانایی الکتریکی همراه بود. منشا فیزیکی این تغییر با استفاده از XPS، همانطور که در بخش 3.2 توضیح داده شد، بررسی شد . بنابراین، اگر قطبیت نادرست به اشتباه اعمال شود، هر الکترود پوشش داده شده با قلع موجود در یک الکترولیز تجاری در معرض خطر تخریب قابل توجهی خواهد بود.
مقایسه عملکرد الکتریکی هر دو کاتد فولاد زنگ نزن و کاتد پوشش داده شده با قلع همانطور که در شکل 2 نشان داده شده است . این نتایج نشان می دهد که شیب های تافل برای هر دو ماده تقریباً یکسان است. هر دو تا حد زیادی موازی با مقدار 120 mV/decade هستند (نشان داده شده به صورت خط چین)، که مقدار پیش بینی شده از محاسبات نظری در ادبیات [ 18 ] است. با این حال، الکترود پوشش داده شده به حدود 300 میلی ولت اضافه پتانسیل اضافی برای دستیابی به چگالی جریان مشابه با مواد بدون پوشش نیاز دارد.
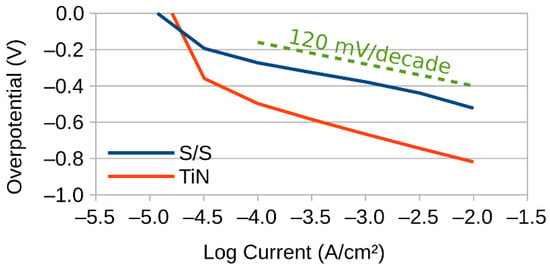
شکل 2. نمودارهای تافل برای فولاد ضد زنگ و قلع قبل از پیری.
شکل 3 نمایش بصری الکترودها را پس از پروتکل پیری الف نشان می دهد. در اینجا می توان دید که کاتد پوشش داده شده با TiN ( شکل 3 e) بیشتر رنگ طلایی اولیه خود را حفظ کرده است، برخلاف فولاد ضد زنگ بدون پوشش ( شکل 3 ج). ، که تقریباً بنفش شد.

شکل 3. ظاهر بصری قبل و بعد از پیری پروتکل A 316 الکترود فولادی ضد زنگ هر دو با قلع و بدون پوشش پوشش داده شده اند. ( A ) الکترود اصلی بدون پیری است، ( B ) و ( C ) به ترتیب آند و کاتد هستند، ( D ) الکترود پوشش داده شده از TiN پیر نشده، ( E ) و ( F ) به ترتیب آند و کاتد هستند.
در طول این آزمایشها، هیچ یک از ترکیبها تغییرات زیادی در عملکرد الکتریکی دو الکترود نشان نداد، همانطور که در شکل 4 نشان داده شده است . این نشان می دهد که هر دو ماده حداقل در این چگالی جریان در طولانی مدت از نظر الکتریکی پایدار هستند. همچنین توجه داشته باشید که سلول TiN به طور مداوم به 250 میلی ولت اضافی نیاز دارد که به خوبی با نتایج سه الکترود ارائه شده در شکل 2 مطابقت دارد . بنابراین ممکن است نتیجه بگیریم که بیشتر این ولتاژ اضافی در نتیجه پوشش TiN روی کاتد است.
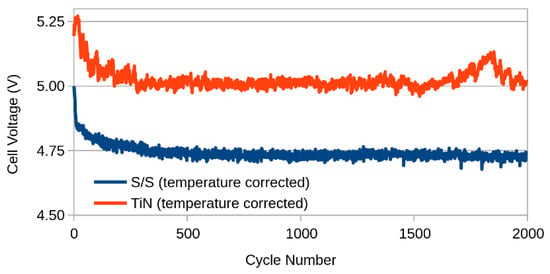
شکل 4. تغییر ولتاژ سلول در 2000 سیکل پروتکل پیری A.
همانطور که در شکل 5 نشان داده شده است ، آزمایشهای طولانیمدت بیشتری در 200 میلی آمپر سانتیمتر مربع انجام شد تا آزمایش شود که آیا عملکرد الکتریکی کاتد فولاد ضد زنگ بدون پوشش در صورت قرار گرفتن در معرض پیری سریعتر، تحلیل میرود .
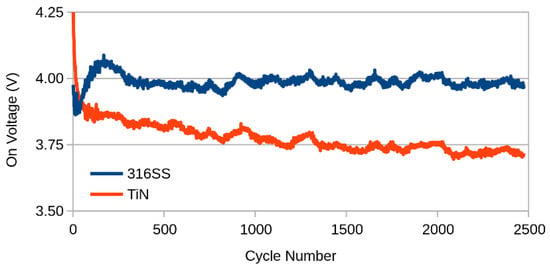
شکل 5. تغییر ولتاژ سلول در 2000 سیکل پروتکل پیری B.
در اینجا مشاهده می شود که به دلیل غلظت بیشتر الکترولیت، ولتاژ به طور کلی کمتر بود. همچنین، اختلاف 300 میلی ولت اولیه به سرعت برگردانده شد، و پس از آن شکاف به تدریج افزایش یافت تا اینکه در نهایت سلول TiN حدود 250 میلی ولت از سلول فولاد ضد زنگ بهتر عمل کرد. این بهبود عملکرد لزوماً قابل انتساب به کاتد نیست، زیرا یک سلول دو الکترودی است، و بنابراین اجازه نمیدهد ارزیابی فردی از هر یک از الکترودها انجام شود. برای ارزیابی این، آزمایشهای سه الکترودی دوباره برای اندازهگیری عملکرد الکتریکی کاتدها به صورت مجزا، همانطور که در شکل 6 نشان داده شده است، انجام شد .
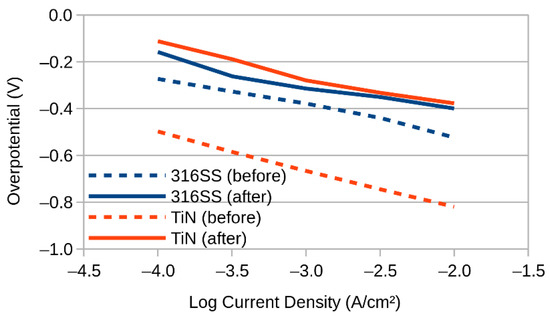
شکل 6. نمودارهای تافل قبل و بعد از پیری پروتکل B.
کاتد TiN اکنون میتوانست از کاتد ضد زنگ بهتر عمل کند، اگرچه تنها حدود 20 میلی ولت. بهبودی که در شکل 5 مشاهده می شود . بنابراین احتمالاً به دلیل عواملی غیر از کاتد به تنهایی است، مانند الکترولیت، غشاء یا آند. شاید بیشترین اهمیت را مشاهده کنیم که آند مورد استفاده در ارتباط با کاتد قلع، ظاهری مسی به خود گرفته است و ممکن است این امر منجر به افزایش غیرمنتظره و غیرقابل توضیح در عملکرد شده باشد. همچنین قابل توجه این است که هر دو کاتد در طول آزمایش بهبود یافتند، با کاهش بیش از حد پتانسیل کاتد TiN به میزان قابل توجهی 400 میلی ولت.
همانطور که در شکل 7 نشان داده شده است، علیرغم این بهبود در عملکرد الکتریکی، هر دو الکترود در ظاهر بصری خود زوال قابل توجهی نشان دادند . با این وجود، شاید نشان دهنده پتانسیل آنها برای طول عمر در دنیای واقعی باشد که ظاهر آنها پس از غوطه ور شدن به مدت سه روز در 0.5 مولار NaOH تازه بهبود یافت (تصاویر سمت راست شکل 7 را ببینید )، علیرغم اینکه بلافاصله پس از افزایش سن تقریباً کاملاً سیاه بودند.

شکل 7. ظاهر بصری قبل و بعد از پیری پروتکل A از 316 کاتد فولادی ضد زنگ هر دو با قلع و بدون پوشش پوشش داده شده اند. ( A ) کاتد اصلی بدون پیری است، ( B ) بلافاصله پس از پیری است، ( C ) پس از 3 روز دیگر در 0.5 مولار NaOH نشسته است، ( D ) کاتد اصلی با پوشش قلع کهنه نشده است، ( E ) بلافاصله پس از پیری است، ( F ) پس از 3 روز دیگر نشستن در 0.5 مولار NaOH است.
3.1. SEM و EDX
کاتدهای شکل 7 . با استفاده از SEM و EDX تجزیه و تحلیل شدند، زیرا طراحی کوچکتر آنها به آنها اجازه می داد در داخل میکروسکوپ الکترونی نصب شوند، با نتایجی که در شکل 8 و جدول 3 ارائه شده است . میکروگراف SEM حضور کریستالها را نشان داد و از طیف EDX بهدستآمده مشخص شد که آنها عمدتاً از مس تشکیل شدهاند. این را می توان به لایه مس اعمال شده در زیر قلع در طول رسوب تجاری نیترید تیتانیوم نسبت داد.

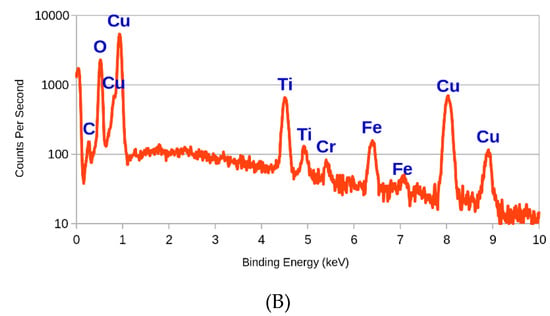
شکل 8. میکروگراف الکترونی با بزرگنمایی 5000 برابری ( A ) و طیف EDX رسوب کریستالی ( B ) برای کاتد نیترید تیتانیوم پس از پروتکل پیری B.
جدول 3. تجزیه و تحلیل کمی طیف EDX فوق برای رسوب کریستالی.

برای کاتد فولاد زنگ نزن، ظاهر مانند شکل 9 بود . تفاوت قابل توجهی بین نیمه بالایی الکترود (محل ‘a’)، که بدون تأثیر به نظر می رسید، و نیمه پایینی (محل ‘b’)، که با ذرات کوچک تقریباً 500 نانومتر پوشیده شده بود، وجود داشت. تجزیه و تحلیل EDX ذرات تایید کرد که 70 درصد وزن آنها مس است.

شکل 9. میکروگراف های الکترونی با بزرگنمایی 5000 برابری کاتد فولاد ضد زنگ پس از پروتکل پیری B.
این با رنگ مسی نمایش داده شده توسط الکترود مطابقت دارد، اما با این وجود یک نتیجه شگفتانگیز است، زیرا هیچ منبع واضحی از مس در آزمایش وجود ندارد. بنابراین حدس زده می شود که سطوح کمی از مس باید در الکترولیت، غشاء یا فولاد ضد زنگ وجود داشته باشد. این توسط نتایج EDX به دست آمده توسط Kao و همکاران پشتیبانی می شود. [ 19 ]، و با آزمایش بر روی نمونههای فولاد زنگ نزن درجه 316 از دو تامینکننده فولاد جداگانه، که در آن درصد مس بین 1 تا 1.6 درصد وزنی مشاهده شد، حتی اگر طبق استانداردهای رسمی، فولاد ضد زنگ درجه 316 حاوی مس نیست. صرف نظر از منبع آلودگی، این نتیجه نشان می دهد که مس تا چه حد می تواند در طول استفاده متناوب روی کاتد بسیار متمرکز شود. با این حال، تأثیر ناچیزی بر عملکرد طولانی مدت الکترود وجود دارد.
3.2. XPS (طیفسنجی فوتوالکترون پرتو ایکس)
همانطور که در بخش 3 مورد بحث قرار گرفت، پوشش TiN در صورتی که حتی برای مدت کوتاهی به عنوان آند استفاده شود، به سرعت دچار زوال می شود . پس از جارو کردن از 0 تا 0.7 ولت در 10 میلی ولت بر ثانیه، پوشش به رنگ نارنجی مایل به قهوه ای تیره تغییر کرد و عملکرد الکتریکی به شدت کاهش یافت. بررسی پوشش اصلی با استفاده از XPS قبل و بعد از این تغییر نتایجی را به همراه داشت که در شکل 10 نشان داده شده است . واضح است که اجزای بیشتری در سیگنال XPS پوشش اصلی TiN وجود دارد.
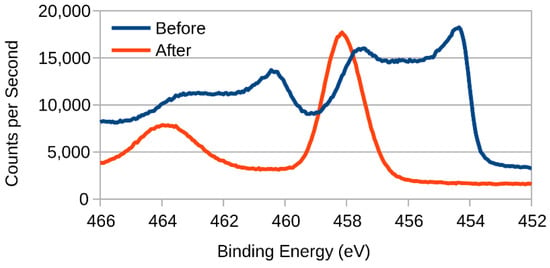
شکل 10. نتایج XPS برای ناحیه Ti 2p قبل و بعد از استفاده به عنوان آند.
به منظور شناسایی این مولفه ها، نتایج با استفاده از نرم افزار CasaXPS که قادر به انجام پیک فیتینگ است، مورد تجزیه و تحلیل قرار گرفت. به طور معمول، همه اوربیتالهای الکترونی 2p یک سیگنال XPS متشکل از دوتایی تولید میکنند که به موجب آن پیک انرژی اتصال پایینتر (2p 1/2 ) مساحت پیک بالاتر (2p 3/2 ) را دو برابر میکند، اما همان نیمه حداکثر عرض کامل را دارد. (FWHM). با این حال، مشخص است که محدودیت FWHM به دلیل اثر Coster-Kronig، که باعث گسترش پیک 2p 1/2 می شود، به طور کامل برای تیتانیوم قابل استفاده نیست [ 20 ]. با این وجود، هنوز هم امکان انجام دکانولوشن پیک طرح کلی وجود دارد که نتایج آن همانطور که در شکل 11 ارائه شده است .
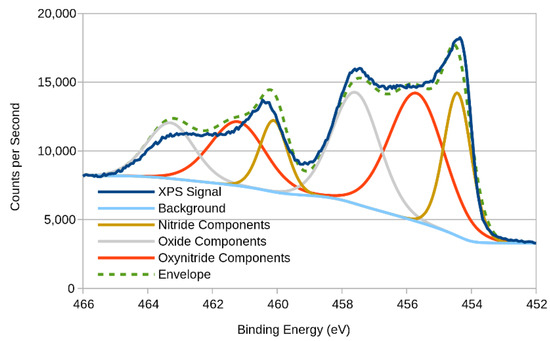
شکل 11. نتایج XPS و برازش اجزا برای منطقه Ti 2p نیترید تیتانیوم.
برازش حضور سه جزء مجزا را در سیگنال کلی XPS نشان میدهد، که مطابق با حضور نیترید و اکسید تیتانیوم [ 10 ، 21 ] و همچنین اکسی نیترید [ 17 ، 20 ] مطابقت دارد. با توجه به موقعیت اجزای باقیمانده در شکل 10 (در ~458 eV)، واضح است که پس از استفاده کوتاه مدت به عنوان آند، لایه های سطحی پوشش تمام آثار نیتروژن را از دست داده و به تیتانیوم اکسید شده تبدیل می شود. این قابل درک است، زیرا آندها به طور کلی مستعد اکسیداسیون هستند و تیتانیوم به طور خاص مستعد اکسیداسیون است [ 20 ]. یافته مشابهی توسط وانگ و همکاران انجام شده است. که مشاهده کردند که هر چه غلظت نیترید در پوشش اکسی نیترید آنها بیشتر باشد، تمایل آن به اکسید شدن برگشت ناپذیر در شرایط آندی بیشتر است [ 22 ].
از آنجایی که XPS یک تکنیک تحلیلی بسیار حساس به سطح است و منحصراً ~10 نانومتر بالایی را بررسی میکند، میتوان از یک پرتو یونی برای آسیاب کردن به سطح استفاده کرد و در نتیجه اطلاعات پروفایل عمق را بدست آورد که نتایج آن در شکل 12 نشان داده شده است. . در اینجا اعداد 1 تا 9 به اندازه گیری های متوالی عمیق تر XPS اشاره دارند و نشان می دهند که پیک نیتروژن با افزایش عمق به تدریج قوی تر می شود.
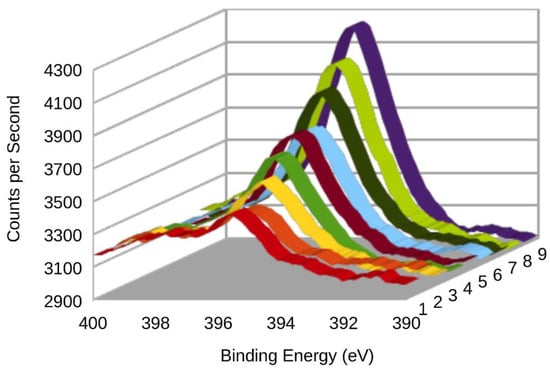
شکل 12. نمایه عمق XPS (با صاف کردن) ناحیه Ti N1s نیترید تیتانیوم تغییر یافته به صورت آندی.
ظهور مجدد پیک نیتروژن نشان می دهد که فولاد ضد زنگ محافظت شده و با قلع در عمق پوشیده شده است، اما به طور کلی الکترود متحمل افت عملکرد الکتریکی ناشی از اکسید روی سطح می شود که در این ولتاژها عایق است [ 22 ]. بنابراین نتیجه گیری می شود که ترکیب فازی پوشش تغییر یافته به صورت آندی از TiOx در سطح، به TiN در عمق، از طریق مخلوطی شامل اکسی نیترید تیتانیوم تغییر می کند ، همانطور که با تغییر به رنگ نارنجی-قهوه ای [ 23 ] و تغییر XPS [ 24 ، 25 ، 26 ]. اهمیت عملی این است که سیم کشی نادرست یا نوسانات در قطبیت ورودی الکتریکی به سرعت تجهیزات الکترولیز را بی اثر می کند. بنابراین، در عمل باید نوعی حفاظت در برابر قطبیت معکوس ارائه شود، به عنوان مثال از طریق استفاده از یک دیود و فیوز، یا در عوض یک ترانزیستور اثر میدان (FET). با این حال، هر دو راه حل، از نظر هزینه یا قابلیت اطمینان، مسئولیتی را به همراه خواهند داشت.
4. نتیجه گیری
بهبود عملکرد الکتریکی و قابلیت اطمینان فولاد ضد زنگ درجه 316 به عنوان کاتد برای تقسیم آب با استفاده از یک پوشش تجاری نیترید تیتانیوم در دسترس بررسی شده است. در ابتدا به نظر می رسد که این افزایش 300 میلی ولتی در مازاد پتانسیل داشته باشد، اما در آزمایش های متناوب طولانی مدت در 200 میلی آمپر سانتی متر مربع ، یک سلول دو الکترودی که پوشش را در خود جای داده بود مشاهده شد که 250 میلی ولت از مواد بدون پوشش بهتر عمل کرد. در این چگالی جریان، هر دو کاتد فولاد ضد زنگ و کاتد TiN تغییر رنگ قابل توجهی را تجربه کردند ( شکل 7 را ببینید ). به نظر می رسد که این تا حدی برگشت پذیر است، زیرا مشاهده می شود که رسوب طی چند روز در الکترولیت حل می شود. مهمتر از آن، مواد پوشش داده شده پس از چنین استفاده متناوب، افزایش قابل توجهی در عملکرد الکتریکی نشان دادند و 400 میلی ولت بهبود یافتند، که برای پیشی گرفتن از مواد بدون پوشش کافی بود. شکل 6 نشان می دهد که ماده پوشش داده شده در یک سیستم سه الکترودی از مواد پوشش داده نشده بهتر عمل کرده است و شکل 5 نشان می دهد که در صورت استفاده به عنوان یک سیستم کامل از مواد پوشش داده شده نیز بهتر عمل کرده است. نتایج SEM در شکل 8 و شکل 9 نشان می دهد که “ظاهر سیاه” هر دو کاتد در واقع دلایل زمینه ای متفاوتی دارد.
شناسایی با استفاده از SEM (میکروسکوپ الکترونی روبشی) تأیید کرد که مهاجرت و رسوب مس ممکن است مسئول برخی از این افزایش باشد. میکروگراف های الکترونی از مواد پوشش داده شده پس از پیری تعداد زیادی کریستال مس با نوک تیز را نشان می دهد. این تئوری وجود دارد که اینها از یک لایه مس که توسط تامین کننده پوشش قبل از اعمال پوشش نیترید تیتانیوم رسوب کرده بود، رشد کردند. برای مواد بدون پوشش، بسیاری از ذرات مس با قطر تقریباً 500 نانومتر مشاهده شد که رسوب کرده اند. در حالی که منبع این آلودگی مس ناشناخته باقی مانده است، ظاهر آنها با کاهش عملکرد مرتبط نیست.
همچنین تأیید شد که TiN به هیچ وجه نمیتواند به عنوان آند استفاده شود، و مشخصهیابی با استفاده از XPS (طیفسنجی فوتوالکترون اشعه ایکس) نشان داد که پوشش تبدیل سریع به TiOx را تجربه میکند ، با از دست دادن تمام نیتروژن از لایههای سطحی. آسیاب پرتو یونی نشان داد که انتقال از TiOx در سطح به TiN در عمق تدریجی است و بنابراین لزوماً ترکیبات واسطه ای از اکسی نیترید تیتانیوم را در بر می گیرد. این امکان وجود دارد که یک ترکیب سه تایی از TiAlN یا CrAlN ممکن است مقاومت بیشتری در برابر اکسیداسیون الکتریکی نشان دهد، همانطور که برای اکسیداسیون حرارتی توسط Chim و همکاران تایید شده است. [ 27 ]. با این وجود، این کار کمی از کاربرد قلع به عنوان کاتد برای تقسیم آب الکترولیتی تحت شرایط قلیایی متناوب دمای اتاق کم می کند.
مشارکت های نویسنده
مفهوم سازی، CWD. روش، CWD; نرم افزار، WJFG; اعتبارسنجی، WJFG; تجزیه و تحلیل رسمی، WJFG; تحقیق، WJFG و DRJ. منابع، CWD; مدیریت داده، CWD؛ نوشتن – آماده سازی پیش نویس اصلی، WJFG. نوشتن – بررسی و ویرایش، WJFG. تجسم، WJFG; نظارت، WJFG; مدیریت پروژه، CWD؛ کسب بودجه، CWD
منابع مالی
دانشجوی دکترا ویلیام گانون، با کمک بورسیه دانشگاه سوانسی زینکیویچ.
قدردانی ها
مایلیم از کمک ارائه شده توسط کالج مهندسی دانشگاه سوانسی AIM Facility که تا حدی توسط EPSRC (EP/M028267/1)، صندوق توسعه منطقه ای اروپا از طریق دولت ولز (80708) و پروژه Sêr Solar تامین مالی شده است، قدردانی کنیم. از طریق دولت ولز WJG از مرکز Zienkiewicz برای کمک مالی دکترا تشکر می کند.
تضاد علاقه
نویسندگان هیچ تضاد منافع را اعلام نمی کنند.